Proposal Penelitian terkait TNBC Type oleh Kelompok TW2201A
DAFTAR ISI:
BAB 1 PENDAHULUAN
-
- Latar Belakang Masalah
- Rumusan Masalah
- Tujuan Penelitian
- Manfaat Penelitian
BAB 2 TINJAUAN PUSTAKA
-
- Breast Cancer
- Triple Negative Breast Cancer (TNBC)
- Trop-2
BAB 3 METODE PENELITIAN
-
- Metode Penelitian
- Prosedur dan Tahapan Penelitian
- Luaran Tiap Tahapan Penelitian
- Indikator Capaian Tiap Tahapan Penelitian
DAFTAR PUSTAKA
BAB 1 PENDAHULUAN
Latar Belakang
Kanker adalah suatu penyakit dimana terjadi pertumbuhan yang tidak terkontrol dari suatu sel tubuh yang kemudian menyebar ke bagian tubuh yang lainnya. Kanker dapat bermula dari setiap bagian tubuh manusia. Sel tubuh manusia bertumbuh dan kemudian rusak sehingga akan digantikan oleh sel-sel tubuh yang baru. Namun terkadang siklus pertumbuhan sel ini rusak dan sel-sel yang sudah rusak bertumbuh dan bereplikasi. Sel-sel ini dapat membentuk tumor.
Kanker payudara merupakan jenis kanker yang paling sering terjadi dan juga merupakan penyebab kematian kedua terbesar karena kanker pada wanita. Pada tahun 2020, terdapat 2,3 juta wanita yang terdiagnosis kanker payudara dan 685,000 kematian secara global. Hingga akhir tahun 2020, ada 7,8 juta wanita hidup yang didiagnosis menderita kanker payudara dalam 5 tahun terakhir, menjadikannya kanker paling umum di dunia. Ada lebih banyak tahun hidup yang disesuaikan dengan disabilitas yang hilang (DALYs) oleh wanita karena kanker payudara secara global daripada jenis kanker lainnya. Kanker payudara terjadi di setiap negara di dunia pada wanita pada usia berapa pun setelah pubertas tetapi dengan tingkat yang meningkat di kemudian hari (WHO, 2020).
Kanker payudara seringkali berkembang tanpa diketahui. Kebanyakan pasien menyadari penyakit mereka saat melakukan pemeriksaan rutin atau secara tidak sengaja mengamati benjolan atau perubahan pada payudara. Kanker payudara mulai berkembang pada sel epitel duktus maupun lobulus jaringan glandula payudara. Sel-sel kanker pada awalnya hanya berkembang pada duktus ataupun lobulus (“in situ”). Seiring berjalannya waktu, sel-sel kanker yang tumbuh in situ dapat berkembang dan menyebar ke jaringan payudara di sekitarnya, kelenjar limpa, dan bahkan ke organ tubuh lain (NCBI, 2021).
Pengobatan kanker payudara akan lebih efektif apabila kanker tersebut dapat didiagnosis secara dini. Pengobatan biasanya terdiri dari gabungan operasi, terapi radiasi, dan terapi obat-obatan (kemoterapi, terapi hormonal, dan/atau terapi target). Terdapat dua prinsip dasar pengobatan kanker yaitu mengurangi kemungkinan rekurensi dan risiko metastasis dari sel-sel kanker. Tindakan operasi dengan atau tanpa menggunakan terapi lain dapat mengontrol sel kanker secara lokal. Saat ada risiko metastasis, akan dilakukan tetapi sistemik seperti terapi hormonal, kemoterapi, terapi target, ataupun kombinasi dari pengobatan-pengobatan tersebut.
Terapi target adalah terapi yang ditargetkan untuk bekerja pada mekanisme molekuler spesifik, yang berperan dalam kelangsungan hidup dan proliferasi sel kanker (Chariton et al, 2016). Targeted therapy pada kanker payudara adalah terapi anti-target, hanya dilakukan di rumah sakit tipe A/B, dan anti-HER2 yang hanya diberikan apabila tes IHK untuk HER2 positif. Lini pertama untuk anti-HER2 adalah Herceptin. Penggunaan anti-VEGF atau m-tor inhibitor tidak dianjurkan (Kemenkes RI, 2020).
Triple Negative Breast Cancer (TNBC) merupakan subtipe kanker payudara yang berdasarkan imunohistokimia (IHC) adalah estrogens receptor (ER) negatif, progesterone receptor (PR) negatif dan human epidermal growth factor receptor 2 (HER2) negatif. TNBC dicirikan oleh profil molekulernya yang unik, sifat agresif, pola metastasis yang berbeda, dan kurangnya terapi yang ditargetkan. Diperkirakan bahwa dari beban kanker payudara di seluruh dunia, sekitar 170.000 kasus adalah TNBC dan menyumbang sekitar 10-20% dari kanker payudara invasif (NCBI, 2013).
Rumusan Masalah
Berdasarkan latar belakang yang sudah dipaparkan di atas, rumusan masalah dapat dirumuskan sebagai berikut:
-
- Bagaimana cara agar tipe kanker TNBC dapat diobati dengan terapi target?
- Apakah modifikasi gen dapat membantu terapi kanker tipe TNBC?
- Bagaimana cara menghambat proliferasi sel kanker payudara menggunakan metode CRISPR dengan trop-2?
Tujuan Penelitian
-
- Dapat melihat modifikasi gen suatu sel yang disebarkan pada proses metastasis sel kanker ketika menyerang sel tersebut.
- Mencari terapi yang lebih efektif untuk tipe kanker TNBC.
- Dapat menganalisis data lebih dalam agar mendapat jawaban yang lebih tepat.
- Dapat menjadi solusi terapi kanker payudara bagi pasien stadium lanjut.
- Dapat menjadi gambaran untuk mendapatkan terapi-terapi lain yang lebih efisien kedepannya.
Manfaat Penelitian
Berdasarkan pemaparan-pemaparan yang sudah disebutkan di atas, diharapkan penelitian ini dapat memberikan beberapa manfaat sebagai berikut:
-
- Secara teoritis, dapat memberikan pemahaman lebih lanjut khususnya bagi mahasiswa Universitas Padjadjaran mengenai kanker tipe TNBC dan dapat memberikan sumbangsih bagi dunia penelitian pada umumnya.
- Secara praktis, dapat menjadi salah satu bentuk terapi yang dapat dipilih, selain terapi-terapi yang sudah ada dan dapat lebih luas lagi dampak positif yang di dapat seorang pasien dengan kanker payudara.
BAB 2 TINJAUAN PUSTAKA
Breast Cancer
Berdasarkan buku Harrison’s Internal Medicine (Abbruzzese et al., 2018), kanker payudara adalah proliferasi ganas dari sel epitel yang melapisi duktus atau lobulus payudara. Breast epithelial malignancies merupakan penyebab kanker paling umum pada wanita setelah kanker kulit. Namun, berkat kemajuan tekonologi pengobatan dan deteksi dini, kematian akibat kanker payudara mulai menurun secara substansial.
Kanker payudara manusia adalah penyakit klonal, kondisi dimana satu sel yang ditransformasi (produk dari serangkaian mutasi) akhirnya mampu mengekspresikan potensi keganasan secara penuh. Dengan demikian, kanker payudara mungkin akan dijumpai untuk waktu yang lama baik sebagai penyakit non-invasif atau penyakit invasif tetapi nonmetastasis.
Kanker payudara dapat dikategorisasikan berdasarkan eksistensi hormon reseptor, yaitu estrogen dan progesteron, pada permukaan sel kanker.
Reseptor Estrogen
Menurut John Hopkins dan National Cancer Institution, secara definisi estrogen merupakan jenis hormon yang dibuat oleh tubuh yang membantu mengembangkan dan mempertahankan karakteristik seks wanita dan pertumbuhan tulang panjang. Estrogen juga dapat dibuat di laboratorium. Digunakan sebagai pengendalian pada kelahiran pengobatan gejala menopause, gangguan menstruasi, osteoporosis, dan kondisi lainnya. Ovarium wanita membuat sebagian besar hormon estrogen, selain itu kelenjar adrenal dan sel-sel lemak juga membuat sejumlah kecil hormon.
Selain mengatur siklus menstruasi, banyak sistem organ, termasuk sistem muskuloskeletal dan kardiovaskular, dan otak dipengaruhi oleh estrogen. Peningkatan insiden kanker payudara pada wanita ini telah dikaitkan dengan paparan estrogen tingkat tinggi yang berkepanjangan, seperti yang terjadi pada menarche dini dan menopause terlambat. Studi tingkat estrogen darah di antara wanita pascamenopause telah menunjukkan bahwa tingkat yang lebih tinggi dikaitkan dengan peningkatan risiko kanker payudara berikutnya (Fernandez dan Russo 2010).
Reseptor Progesteron
Menurut National Cancer Institution, secara definisi progesteron mereupakan hormon yang dibuat oleh tubuh yang berperan dalam siklus menstruasi dan kehamilan, dan dapat dibuat di laboratorium (progestin). Serupa dengan estrogen, progesteron dapat digunakan sebagai jenis pengendalian kelahiran dan untuk mengobati gangguan menstruasi, infertilitas, gejala menopause, dan kondisi lainnya.
Progesteron juga merupakan hormon steroid endogen yang umumnya diproduksi oleh korteks adrenal serta gonad, yang terdiri dari ovarium dan testis. Selain itu, ia juga disekresikan oleh korpus luteum ovarium selama sepuluh minggu pertama kehamilan, diikuti oleh plasenta pada fase akhir kehamilan.
Berdasarkan studi Tarbert dkk. (2020), hormon memiliki peran penting dalam mengendalikan proliferasi fisiologis epitel payudara normal, dan karena itu progesteron dapat mempengaruhi kejadian awal karsinogenesis payudara. Progesteron sintetis (progestin) telah dikaitkan dengan peningkatan risiko kanker payudara. Namun, peran progesteron endogen dalam fisiologi payudara dan karsinogenesis masih kurang jelas. Studi mekanistik menggunakan kultur sel, kultur jaringan, dan model praklinis melibatkan progesteron dalam karsinogenesis payudara
Triple Negative Breast Cancer (TNBC)
Berdasarkan American Cancer Society (2022), Triple Negative Breast Cancer (TNBC) merupakan salah satu tipe kanker payudara yang menyumbang sekitar 10-15% kasus dari semua kasus kanker payudara. Istilah Triple Negative Breast Cancer (TNBC) ini mengacu pada fakta bahwa sel kanker tidak memiliki 3 reseptor tidak memiliki reseptor yang biasa ditemukan pada kanker payudara, yaitu estrogen atau progesteron (ER atau PR) dan tidak memiliki protein human epidermal growth factor (HER2). Kanker ini cenderung lebih sering terjadi pada wanita yang lebih muda dari usia 40 tahun, wanita yang berkulit hitam, atau wanita yang memiliki mutasi BRCA1.
TNBC berbeda dari jenis kanker payudara invasif lainnya karena cenderung tumbuh dan menyebar lebih cepat, memiliki lebih sedikit pilihan pengobatan, dan cenderung memiliki prognosis (hasil) yang lebih buruk. TNBC memiliki lebih sedikit pilihan pengobatan dibandingkan dengan jenis kanker payudara lainnya karena sel kanker tidak memiliki reseptor estrogen atau progesteron atau protein HER2 yang cukup untuk membuat terapi hormon atau obat HER2 yang ditargetkan bekerja. Karena terapi hormon dan obat anti-HER2 bukanlah pilihan bagi wanita dengan TNBC, pengobatan yang sering digunakan adalah kemoterapi.
Trop-2
Trop-2 atau yang biasa dikenal dengan trofoblas antigen 2, merupakan glikoprotein transmembran yang dikode oleh Tacsd2gen. Trop-2 dapat diekspresikan pada berbagai jenis sel, termasuk pada sel yang ada pada jaringan normal. Namun, berkebalikan dengan hal tersebut, Trop-2 diekspresikan secara berlebih pada sel kanker. Hal ini disebabkan karena Trop-2 terlibat dalam beberapa jalur pensinyalan sel, termasuk dalam memberikan sinyal bagi sel untuk melakukan pembaruan diri, proliferasi, invasi, dan kelangsungan hidup. Hal ini menjelaskan mengapa ekspresi yang berlebih dapat menyebabkan perkembangan tumor dan jumlah yang banyak dapat menjadi tanda bahwa adanya pertumbuhan sel yang abnormal (Shvartsur & Bonavida, 2015).
BAB 3 METODE PENELITIAN
Metode Penelitian
Metode penelitian yang digunakan dalam penelitian ini adalah dengan melakukan studi eksperimental berbasis laboratorium. Penelitian ini dilakukan secara in-vitro. Sel kanker yang diuji pada penelitian ini adalah jenis triple-negative breast cancer. Ukuran sampel pada penelitian adalah sebanyak 12 sampel, dengan rincian 3 sampel sel TNBC yang dihilangkan gen TACSTD2, 3 sampel sel TNBC yang gen TACSTD2-nya digantikan dengan gen TACSTD1, 3 sampel sel TNBC yang diterapi menggunakan antibody-drug conjugate (sacituzumab govitecan), dan 3 sampel sel TNBC yang tidak diberikan terapi apapun sebagai kontrol. Penjelasan umum dalam penelitian ini adalah sebagai berikut: sel TNBC akan diperoleh dari biopsi salah satu pasien yang mengidap kanker payudara jenis TNBC. Sel TNBC kemudian akan diisolasi dalam 12 tabung kultur sel. 3 tabung berisi TNBC akan diberikan perlakuan berupa pengeliminasian gen TACSTD2-nya melalui CRISPr-Cas9. Pada 3 tabung lainnya akan dilakukan penggantian gen TACSTD2-nya dengan gen TACSTD1 melalui CRISPr-Cas9. Kemudian, 3 sampel lainnya akan diperlakukan dengan pemberian sacituzumab govitecan. Sedangkan, 3 sampel terakhir tidak akan diberikan perlakuan apapun sebagai kontrolnya. Tiga hari setelah perlakuan tersebut, pertumbuhan dan perkembangan sel TNBC dari masing-masing sampel akan dianalisis.
Prosedur dan Tahapan Penelitian
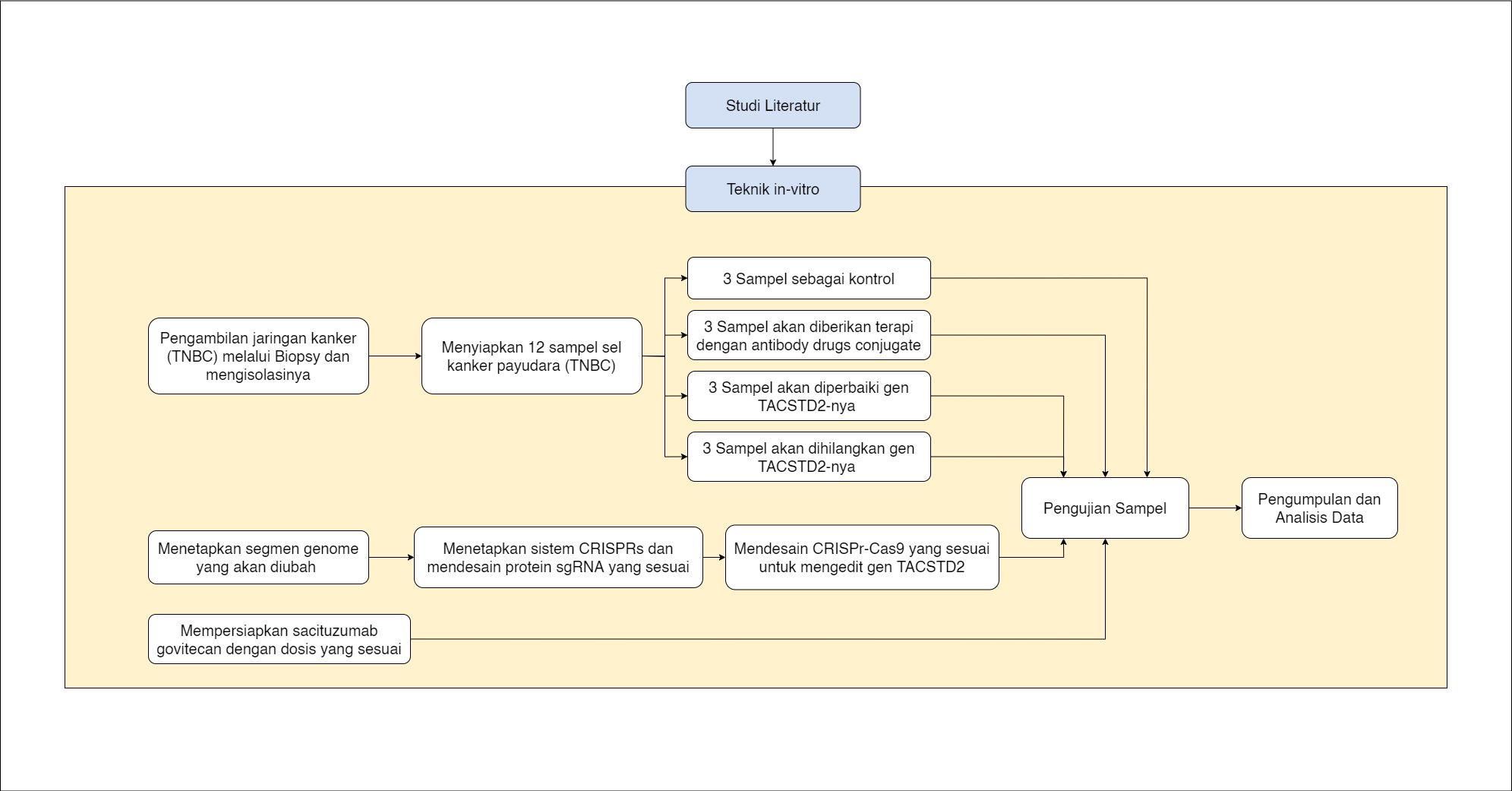
Luaran Tiap Tahapan Penelitian
Adapun luaran yang diharapkan pada tahapan penelitian ini antara lain:
-
- Dihasilkan kompleks CRISPr-Cas9 dengan rantai komplementer yang sesuai dengan gen TACSTD2.
- Dihasilkan isolasi sel TNBC yang diambil dari hasil biopsi.
- Perbandingan pertumbuhan sel TNBC dari sampel-sampel yang diedit gennya, diterapi dengan antibody drugs conjugate, dan tidak diberikan perlakuan apapun.
- Pengeditan gen melalui CRISPr-Cas 9 dapat menekan atau bahkan menghentikan tingkat proliferasi sel TNBC secara signifikan.
Indikator Capaian Tiap Tahapan Penelitian
Adapun indikator capaian dari setiap tahapan penelitian ini antara lain:
-
- Terbentuknya kompleks CRISPr-Cas9 dengan rantai komplementer yang sesuai dengan gen TACSTD2.
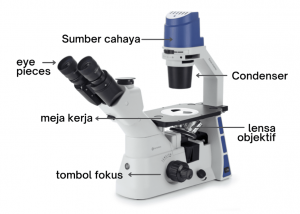
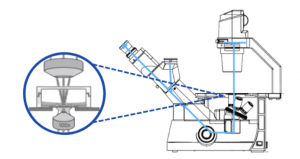
- Terisolasinya sel TNBC dari hasil biopsi dibuktikan dengan pengamatan melalui mikroskop inversi.
- Diperolehnya data perbandingan pertumbuhan sel TNBC dari setiap sampel melalui penghitungan sel-sel TNBC yang masih aktif menggunakan FACS.
- Perbedaan yang signifikan secara statistik antara kelompok sampel yang mengalami pengeditan gen dan tidak.
DAFTAR PUSTAKA
Abbruzzese, J. L., Abdelmalek, M. F., Achermann, J. C., & Adamson, J. W. (2018). Harrison’s Principles in Internal Medicine 20th Edition. https://books.google.com/books/about/Harrison_s_Principles_of_Internal_Medici.html?id=ID5lDwAAQBAJ
Definition of estrogen – NCI Dictionary of Cancer Terms – NCI. (n.d.). Retrieved September 7, 2022, from https://www.cancer.gov/publications/dictionaries/cancer-terms/def/estrogen
Definition of progesterone – NCI Dictionary of Cancer Terms – NCI. (n.d.). Retrieved September 7, 2022, from https://www.cancer.gov/publications/dictionaries/cancer-terms/def/progesterone
Estrogen’s Effects on the Female Body | Johns Hopkins Medicine. (n.d.). Retrieved September 7, 2022, from https://www.hopkinsmedicine.org/health/conditions-and-diseases/estrogens-effects-on-the-female-body
Fernandez, S. V., & Russo, J. (2010). Estrogen and Xenoestrogens in breast cancer. Toxicologic Pathology, 38(1), 110–122. https://doi.org/10.1177/0192623309354108
Shvartsur, A., & Bonavida, B. (2015). Trop2 and its overexpression in cancers: regulation and clinical/therapeutic implications. Genes & Cancer, 6(3–4), 84. https://doi.org/10.18632/GENESANDCANCER.40
Trabert, B., Sherman, M. E., Kannan, N., & Stanczyk, F. Z. (2020). Progesterone and Breast Cancer. https://doi.org/10.1210/endrev/bnz001
Triple-negative Breast Cancer | Details, Diagnosis, and Signs. (2022). Retrieved September 7, 2022, from https://www.cancer.org/cancer/breast-cancer/about/types-of-breast-cancer/triple-negative.html
Proposal penelitian ini dibuat secara berkelompok yaitu kelompok TW2201 yang dibimbing oleh bu Nayla Majeda Alfarafisa, Ph.D, dengan anggota, antara lain:
-
- Kemal Malik Pasha
- Zahra Fauziah Rifani
- Riordan Sherwyn Almathea Wibowo
- Nurjanah Sriyanti
- Amara Tunggadewi Ayu Pramesti
- Geubrina Raesuki
- Olivia Pramesthi Cahyarini
- Fatiya Adila Refah Rachman